
Il modello atomico di Rutherford o modello atomico planetario è un modello dell'atomo proposto da Ernest Rutherford. Rutherford diresse l'esperimento di Geiger e Marsden (anche noto, appunto, come esperimento di Rutherford) nel 1909; l'analisi compiuta da Rutherford stesso nel 1911 suggerì che il modello atomico a panettone di J. J. Thomson non era corretto. Il nuovo modello proposto da Rutherford aveva delle caratteristiche che sono rimaste anche in modelli successivi come la concentrazione della maggioranza della materia in un volume relativamente piccolo rispetto alle dimensioni atomiche (ossia un nucleo atomico) e la presenza di elettroni rotanti intorno ad esso, come i pianeti del sistema solare attorno al sole.
Anche se all’inizio gli elettroni vennero associati unicamente alle correnti elettriche, nel giro di pochi anni fu dimostrato, attraverso le misure di radioattività, che essi dovevano essere parte integrante degli atomi. Emerse di conseguenza l’ipotesi che all’interno dell’atomo dovesse esistere una corrispondente carica positiva. Thomson stesso suggerì l’idea che l’atomo fosse costituito da una sfera di carica positiva, in cui gli elettroni erano disseminati «come l’uvetta nel panettone».
Lo scienziato neozelandese Ernest Rutherford e i suoi collaboratori Geiger e Marsden, dopo aver determinato la natura delle radiazioni α (atomi di elio privi di due elettroni), le utilizzarono per bombardare gli atomi d’oro di una sottilissima lamina, dello spessore di 0,01 mm. Dopo l’urto con gli atomi di oro, le particelle α, circa 10 000 volte più pesanti di un elettrone, ma del tutto invisibili all’occhio umano, venivano raccolte da un apposito schermo capace di evidenziare la loro presenza. I risultati dell’esperimento furono i seguenti:
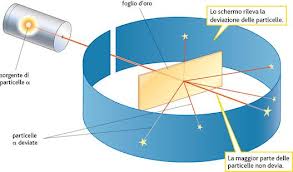
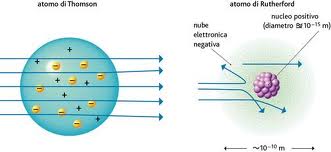
Grazie alla misura degli angoli di deflessione e all’applicazione della legge di Coulomb, Rutherford propose per l’atomo il seguente modello:
A differenza del modello proposto da Thomson, l’atomo di Rutherford è in grado di spiegare i dati raccolti sperimentalmente. Infatti, le poche particelle α che arrivano molto vicino al nucleo sono respinte violentemente dalla sua carica positiva, come se fosse un muro impenetrabile, e tornano indietro. Quasi tutte le altre sono invece soltanto deflesse, o proseguono indisturbate, perché lontano dal nucleo la forza repulsiva è minore ed è attenuata dalla presenza degli elettroni.
Vedi modello atomico di Dalton